21/04/2026
La ANMAT restringió el tránsito de medicamentos a una distribuidora farmacéutica por múltiples incumplimientos
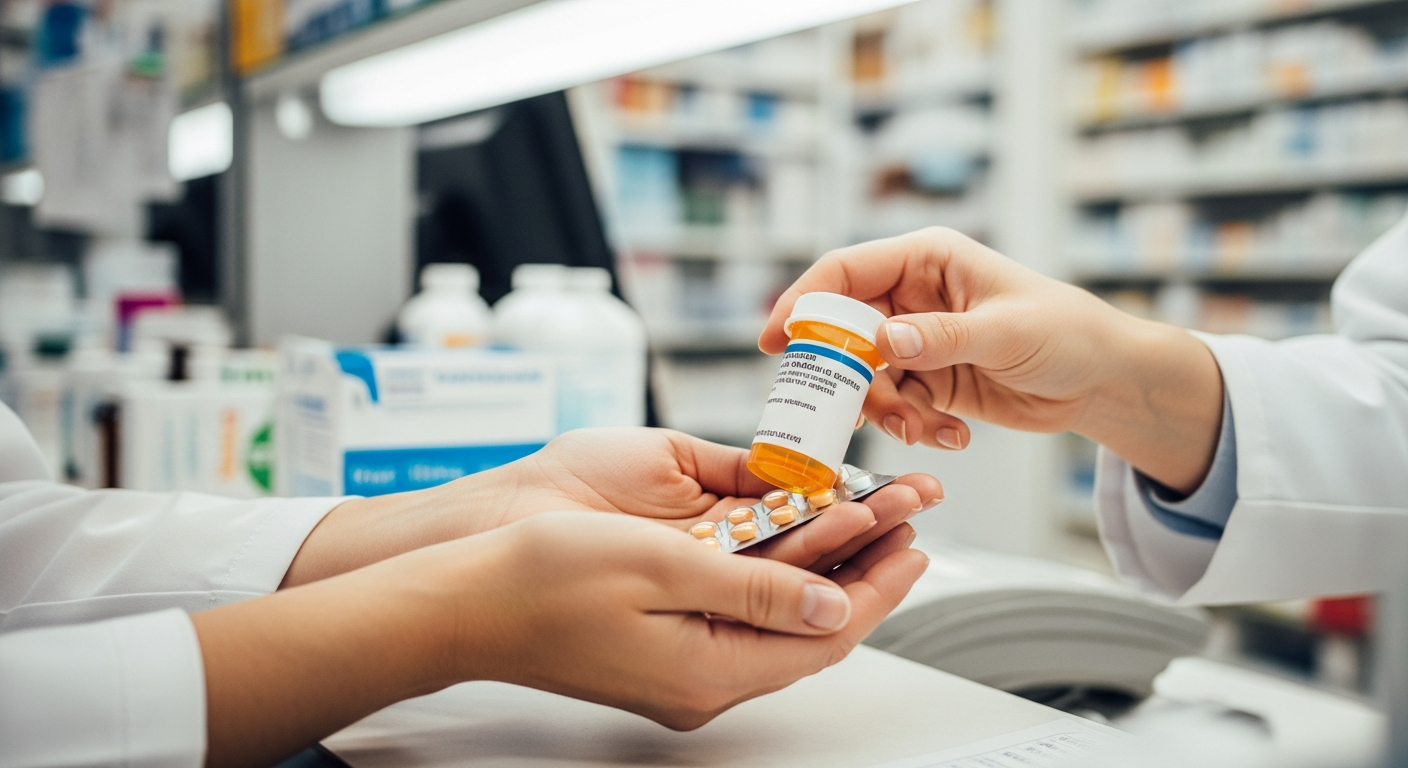
Fuente: telam
Durante una inspección en las instalaciones de la firma Global Pharma Group S.A., el organismo detectó irregularidades que frenaron la renovación del certificado de Buenas Prácticas
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) dispuso la suspensión preventiva de la habilitación para el tránsito interjurisdiccional de medicamentos y especialidades medicinales a la empresa Global Pharma Group S.A., ubicada en el partido de La Matanza.
La decisión se adoptó tras una inspección realizada a principios de febrero donde se detectaron múltiples incumplimientos a las Buenas Prácticas de Distribución de Medicamentos. El procedimiento derivó del trámite de renovación de la habilitación que la firma había iniciado en 2022.
Durante la fiscalización en la localidad de Ramos Mejía donde se encuentra instalada, la comisión inspectora detectó varias irregularidades. Entre ellas aparecía que el portón de ingreso presentaba una abertura que podía facilitar el acceso de insectos, además de acumulación de suciedad en el piso. El organismo indicó que "los locales deben estar diseñados y equipados de manera que minimicen la entrada de insectos, roedores u otros animales. Debe contar con un programa preventivo de control de plagas".
En otro orden, hallaron manchas de humedad y pintura descascarada en la zona de recepción y expedición, junto con la falta de placas ignífugas en el techo del área. "Todas las áreas, independientemente de su uso, deben mantenerse limpias, ordenadas, secas, libres de materiales y elementos extraños, polvo, suciedad o basura", señalaron en la disposición 2028/2026 publicada en la madrugada de hoy.
Además, describieron que en el control de temperaturas se verificaron desviaciones significativas en los registros tanto en el depósito como en la heladera destinada a medicamentos, superando los valores permitidos y sin contar con evidencia documental de control de alarmas. Entre el cúmulo de irregularidades, el organismo señaló una desactualización en el sistema informático utilizado. Según el texto oficial, este no permitía el rastreo por lote para productos sin soporte físico de trazabilidad, y la documentación emitida carecía de detalles.
La empresa tampoco había realizado un mapeo térmico del depósito, requerido para asegurar zonas aptas para almacenamiento; y durante una simulación de armado de un pedido para productos que requieren cadena de frío, observaron temperaturas por debajo de 2�C durante un lapso considerable, lo que no se ajusta a los requerimientos normativos.
ANMAT indicó irregularidades en los procedimientos operativos estándar como "transporte, control de temperatura en depósitos y cadena de frío, calificación de proveedores, retiros de mercado". En relación a los clientes, se encontraron archivos incompletos respecto a las habilitaciones sanitarias, contraviniendo la obligación de verificar la cadena legal de abastecimiento. En función de todas estas observaciones, la Dirección de Evaluación y Gestión de Monitoreo de Productos para la Salud notificó a la empresa que no emitirán el certificado hasta que se verifique el cumplimiento integral de las Buenas Prácticas. Los incumplimientos observados no pudieron ser subsanados durante el transcurso de la inspección y se mantendrán hasta tanto se verifique que la empresa realizó los arreglos pertinentes.
De esta manera, la disposición afirmó: "Suspéndase preventivamente la habilitación para efectuar tránsito interjurisdiccional de medicamentos y especialidades medicinales a la firma GLOBAL PHARMA GROUP S.A., Legajo N� 995, CUIT N� 30-71519153-5, con domicilio en la calle Rondeau 1418 de la localidad de Ramos Mejía, partido de La Matanza, provincia de Buenos Aires".
Si bien la firma había presentado previamente documentación la misma resultó insuficiente para levantar la medida. Además, se inició un sumario sanitario a la empresa y a su directora técnica, por presuntas infracciones a la Ley N� 16.463, la Disposición ANMAT N� 2069/2018 y otras normativas concordantes. El mismo fue comunicado a la Dirección de Gestión de Información Técnica para su registro y publicación, así como a las autoridades sanitarias nacionales y provinciales, y a las áreas correspondientes del Ministerio de Salud.
Fuente: telam